QUÍMICA ORGÂNICA II
Aldeídos e cetonas reagem com aminas primárias levando à formação de iminas. Esses compostos são bastantes utilizados como intermediários na síntese de produtos de ocorrência natural com estruturas mais complexas. Porém se reagirmos um aldeído ou cetona com uma amina secundária, teremos a formação de uma:
Amina aromática.
Enamina.
Amida.
Amina primária.
Imina.
Substâncias químicas, como o hidreto de lítio e alumínio e boroidreto de sódio são agentes redutores mais utilizados em síntese orgânica. Processando-se a reação de redução entre a propanona e hidreto de lítio e alumínio qual será o produto formado? Escolha a alternativa que apresenta o produto da reação.
Propanol-2
Propanona-2
Propeno
Propano
Propanal-2
O polímero dacron, usado na fabricação de tecidos, é obtido pela condensação de etilenoglicol com ácido tereftálico mostrado, a seguir:
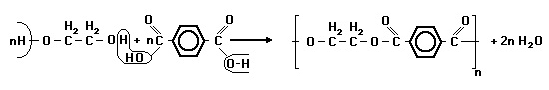 Na estrutura do polímero caracteriza-se a função:
Na estrutura do polímero caracteriza-se a função:
Anidrido de ácido.
Aldeído.
Éter.
Cetona.
Éster.
Os anidridos de ácidos carboxílicos são compostos que apresentam em sua estrutura química um átomo de oxigênio ligado a dois grupos carbonílicos com dois radicais orgânicos. Sobre os anidridos, marque a alternativa correta.
Se as duas moléculas de ácido carboxílico que formam o anidrido forem diferentes, o anidrido será chamado de simétrico.
Se as duas moléculas de ácido carboxílico que formam o anidrido forem iguais, o anidrido será chamado de assimétrico.
Os anidridos mistos são nomeados mantendo o nome de apenas um ácido carboxílico.
Os anidridos simétricos são nomeados pelo nome do ácido carboxílico correspondente.
A palavra anidrido significa com água.
As reações abaixo podem ocorrer através de substituições nucleofílicas do tipo Sn1 ou Sn2. A reação de substituição classificada como Sn1 ocorre via formação de carbocátion, e a Sn2, o nucleófilo faz o ataque por trás do grupo abandonador formando um produto com configuração invertida. Considerando os conceitos de substituição nucleofílica, com relação à classificação das reações 1 e 2 abaixo e a natureza do grupo abandonador cloro, pode-se afirmar que:
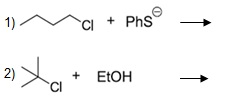
Sn2 e Sn1; o cloro sai na forma de Cl- pelo fato de ser uma base fraca.
Sn1 e Sn2; o cloro é um bom grupo abandonador, pois forma uma base estável.
Sn1 e Sn2; o cloro não é um bom grupo abandonador porque forma uma base instável.
Sn1 e Sn1; o cloro sai na forma de Cl- e pode ser considerado uma base forte.
Sn2 e Sn2; o cloro é um bom grupo abandonador, pois forma uma base estável.
Qual a ordem decrescente de reatividade em condições de SN2 para os seguintes substratos:
- 1-cloro-2-metilbutano
- 2-cloro-2-metilbutano
- 1-cloro-3metilbutano
- 1-cloro-pentano
1-cloro-2-metilbutano, 1-cloro-3-metilbutano, 2-cloro-2-metilbutano, 1-cloro-pentano
1-cloro-pentano, 1-cloro-2-metilbutano, 2-cloro-2-metilbutano, 1-cloro-3-metilbutano
1-cloro-3-metilbutano, 1-cloro-2-metilbutano, 2-cloro-2-metilbutano, 1-cloro-pentano
1-cloro-pentano, 1-cloro-3-metilbutano, 1-cloro-2-metilbutano, 2-cloro-2-metilbutano
2-cloro-2-metilbutano, 1-cloro-2-metilbutano, 1-cloro-3-metilbutano, 1-cloro-pentano
Os carbocátions são classificados de acordo com o número de substituintes que estão ligados ao carbono com a carga positiva. Sendo assim carbocátion primário possui apenas um substituinte alquila ligado ao carbono de carga positiva, carbocátion secundário possui dois substituintes ligados e carbocátion terciário possui três substituintes ao carbono com carga positiva. Sendo assim, podemos afirmar que a estabilidade do carbocátion:
Diminui com o aumento de substituintes ao carbono com carga positiva.
Aumenta com o aumento de substituintes ao carbono com carga positiva.
O carbocátion possui sempre a mesma estabilidade.
Aumenta com o menor número de substituintes ao carbono com carga positiva.
Aumenta com o aumento de substituintes ao carbono com carga negativa.
Para compreender as reações químicas orgânicas, devemos conhecer primeiramente alguns conceitos básicos, como diferenciar nucleófilos de eletrófilos. Sendo assim, analisando as espécies químicas a seguir:
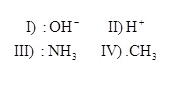 Podemos dizer que estas podem ser classificadas, respectivamente, como:
Podemos dizer que estas podem ser classificadas, respectivamente, como:
Radical livre, reagente nucleófilo, reagente nucleófilo, reagente eletrófilo.
Reagente nucleófilo, radical livre, reagente nucleófilo, reagente eletrófilo.
Reagente nucleófilo, reagente eletrófilo, reagente nucleófilo, radical livre.
Reagente eletrófilo, reagente nucleófilo, reagente nucleófilo, radical livre.
Reagente eletrófilo, radical livre, reagente nucleófilo, reagente nucleófilo.
Pelo conceito de Lewis, base é toda espécie química capaz de doar par de elétrons, enquanto que um ácido, é a espécie que está deficiente de elétrons e poderá receber esse par. Assinale, entre as alternativas abaixo, a fórmula de um composto que é uma base de Lewis:
Amina aromática.
Enamina.
Amida.
Amina primária.
Imina.
Substâncias químicas, como o hidreto de lítio e alumínio e boroidreto de sódio são agentes redutores mais utilizados em síntese orgânica. Processando-se a reação de redução entre a propanona e hidreto de lítio e alumínio qual será o produto formado? Escolha a alternativa que apresenta o produto da reação.
Propanol-2
Propanona-2
Propeno
Propano
Propanal-2
O polímero dacron, usado na fabricação de tecidos, é obtido pela condensação de etilenoglicol com ácido tereftálico mostrado, a seguir:
 Na estrutura do polímero caracteriza-se a função:
Na estrutura do polímero caracteriza-se a função:
Anidrido de ácido.
Aldeído.
Éter.
Cetona.
Éster.
Os anidridos de ácidos carboxílicos são compostos que apresentam em sua estrutura química um átomo de oxigênio ligado a dois grupos carbonílicos com dois radicais orgânicos. Sobre os anidridos, marque a alternativa correta.
Se as duas moléculas de ácido carboxílico que formam o anidrido forem diferentes, o anidrido será chamado de simétrico.
Se as duas moléculas de ácido carboxílico que formam o anidrido forem iguais, o anidrido será chamado de assimétrico.
Os anidridos mistos são nomeados mantendo o nome de apenas um ácido carboxílico.
Os anidridos simétricos são nomeados pelo nome do ácido carboxílico correspondente.
A palavra anidrido significa com água.
As reações abaixo podem ocorrer através de substituições nucleofílicas do tipo Sn1 ou Sn2. A reação de substituição classificada como Sn1 ocorre via formação de carbocátion, e a Sn2, o nucleófilo faz o ataque por trás do grupo abandonador formando um produto com configuração invertida. Considerando os conceitos de substituição nucleofílica, com relação à classificação das reações 1 e 2 abaixo e a natureza do grupo abandonador cloro, pode-se afirmar que:

Sn2 e Sn1; o cloro sai na forma de Cl- pelo fato de ser uma base fraca.
Sn1 e Sn2; o cloro é um bom grupo abandonador, pois forma uma base estável.
Sn1 e Sn2; o cloro não é um bom grupo abandonador porque forma uma base instável.
Sn1 e Sn1; o cloro sai na forma de Cl- e pode ser considerado uma base forte.
Sn2 e Sn2; o cloro é um bom grupo abandonador, pois forma uma base estável.
Qual a ordem decrescente de reatividade em condições de SN2 para os seguintes substratos:
- 1-cloro-2-metilbutano
- 2-cloro-2-metilbutano
- 1-cloro-3metilbutano
- 1-cloro-pentano
1-cloro-2-metilbutano, 1-cloro-3-metilbutano, 2-cloro-2-metilbutano, 1-cloro-pentano
1-cloro-pentano, 1-cloro-2-metilbutano, 2-cloro-2-metilbutano, 1-cloro-3-metilbutano
1-cloro-3-metilbutano, 1-cloro-2-metilbutano, 2-cloro-2-metilbutano, 1-cloro-pentano
1-cloro-pentano, 1-cloro-3-metilbutano, 1-cloro-2-metilbutano, 2-cloro-2-metilbutano
2-cloro-2-metilbutano, 1-cloro-2-metilbutano, 1-cloro-3-metilbutano, 1-cloro-pentano
Os carbocátions são classificados de acordo com o número de substituintes que estão ligados ao carbono com a carga positiva. Sendo assim carbocátion primário possui apenas um substituinte alquila ligado ao carbono de carga positiva, carbocátion secundário possui dois substituintes ligados e carbocátion terciário possui três substituintes ao carbono com carga positiva. Sendo assim, podemos afirmar que a estabilidade do carbocátion:
Diminui com o aumento de substituintes ao carbono com carga positiva.
Aumenta com o aumento de substituintes ao carbono com carga positiva.
O carbocátion possui sempre a mesma estabilidade.
Aumenta com o menor número de substituintes ao carbono com carga positiva.
Aumenta com o aumento de substituintes ao carbono com carga negativa.
Para compreender as reações químicas orgânicas, devemos conhecer primeiramente alguns conceitos básicos, como diferenciar nucleófilos de eletrófilos. Sendo assim, analisando as espécies químicas a seguir:
 Podemos dizer que estas podem ser classificadas, respectivamente, como:
Podemos dizer que estas podem ser classificadas, respectivamente, como:
Radical livre, reagente nucleófilo, reagente nucleófilo, reagente eletrófilo.
Reagente nucleófilo, radical livre, reagente nucleófilo, reagente eletrófilo.
Reagente nucleófilo, reagente eletrófilo, reagente nucleófilo, radical livre.
Reagente eletrófilo, reagente nucleófilo, reagente nucleófilo, radical livre.
Reagente eletrófilo, radical livre, reagente nucleófilo, reagente nucleófilo.
Pelo conceito de Lewis, base é toda espécie química capaz de doar par de elétrons, enquanto que um ácido, é a espécie que está deficiente de elétrons e poderá receber esse par. Assinale, entre as alternativas abaixo, a fórmula de um composto que é uma base de Lewis:
Propanol-2
Propanona-2
Propeno
Propano
Propanal-2
O polímero dacron, usado na fabricação de tecidos, é obtido pela condensação de etilenoglicol com ácido tereftálico mostrado, a seguir:
 Na estrutura do polímero caracteriza-se a função:
Na estrutura do polímero caracteriza-se a função:
Anidrido de ácido.
Aldeído.
Éter.
Cetona.
Éster.
Os anidridos de ácidos carboxílicos são compostos que apresentam em sua estrutura química um átomo de oxigênio ligado a dois grupos carbonílicos com dois radicais orgânicos. Sobre os anidridos, marque a alternativa correta.
Se as duas moléculas de ácido carboxílico que formam o anidrido forem diferentes, o anidrido será chamado de simétrico.
Se as duas moléculas de ácido carboxílico que formam o anidrido forem iguais, o anidrido será chamado de assimétrico.
Os anidridos mistos são nomeados mantendo o nome de apenas um ácido carboxílico.
Os anidridos simétricos são nomeados pelo nome do ácido carboxílico correspondente.
A palavra anidrido significa com água.
As reações abaixo podem ocorrer através de substituições nucleofílicas do tipo Sn1 ou Sn2. A reação de substituição classificada como Sn1 ocorre via formação de carbocátion, e a Sn2, o nucleófilo faz o ataque por trás do grupo abandonador formando um produto com configuração invertida. Considerando os conceitos de substituição nucleofílica, com relação à classificação das reações 1 e 2 abaixo e a natureza do grupo abandonador cloro, pode-se afirmar que:

Sn2 e Sn1; o cloro sai na forma de Cl- pelo fato de ser uma base fraca.
Sn1 e Sn2; o cloro é um bom grupo abandonador, pois forma uma base estável.
Sn1 e Sn2; o cloro não é um bom grupo abandonador porque forma uma base instável.
Sn1 e Sn1; o cloro sai na forma de Cl- e pode ser considerado uma base forte.
Sn2 e Sn2; o cloro é um bom grupo abandonador, pois forma uma base estável.
Qual a ordem decrescente de reatividade em condições de SN2 para os seguintes substratos:
- 1-cloro-2-metilbutano
- 2-cloro-2-metilbutano
- 1-cloro-3metilbutano
- 1-cloro-pentano
1-cloro-2-metilbutano, 1-cloro-3-metilbutano, 2-cloro-2-metilbutano, 1-cloro-pentano
1-cloro-pentano, 1-cloro-2-metilbutano, 2-cloro-2-metilbutano, 1-cloro-3-metilbutano
1-cloro-3-metilbutano, 1-cloro-2-metilbutano, 2-cloro-2-metilbutano, 1-cloro-pentano
1-cloro-pentano, 1-cloro-3-metilbutano, 1-cloro-2-metilbutano, 2-cloro-2-metilbutano
2-cloro-2-metilbutano, 1-cloro-2-metilbutano, 1-cloro-3-metilbutano, 1-cloro-pentano
Os carbocátions são classificados de acordo com o número de substituintes que estão ligados ao carbono com a carga positiva. Sendo assim carbocátion primário possui apenas um substituinte alquila ligado ao carbono de carga positiva, carbocátion secundário possui dois substituintes ligados e carbocátion terciário possui três substituintes ao carbono com carga positiva. Sendo assim, podemos afirmar que a estabilidade do carbocátion:
Diminui com o aumento de substituintes ao carbono com carga positiva.
Aumenta com o aumento de substituintes ao carbono com carga positiva.
O carbocátion possui sempre a mesma estabilidade.
Aumenta com o menor número de substituintes ao carbono com carga positiva.
Aumenta com o aumento de substituintes ao carbono com carga negativa.
Para compreender as reações químicas orgânicas, devemos conhecer primeiramente alguns conceitos básicos, como diferenciar nucleófilos de eletrófilos. Sendo assim, analisando as espécies químicas a seguir:
 Podemos dizer que estas podem ser classificadas, respectivamente, como:
Podemos dizer que estas podem ser classificadas, respectivamente, como:
Radical livre, reagente nucleófilo, reagente nucleófilo, reagente eletrófilo.
Reagente nucleófilo, radical livre, reagente nucleófilo, reagente eletrófilo.
Reagente nucleófilo, reagente eletrófilo, reagente nucleófilo, radical livre.
Reagente eletrófilo, reagente nucleófilo, reagente nucleófilo, radical livre.
Reagente eletrófilo, radical livre, reagente nucleófilo, reagente nucleófilo.
Pelo conceito de Lewis, base é toda espécie química capaz de doar par de elétrons, enquanto que um ácido, é a espécie que está deficiente de elétrons e poderá receber esse par. Assinale, entre as alternativas abaixo, a fórmula de um composto que é uma base de Lewis:
Anidrido de ácido.
Aldeído.
Éter.
Cetona.
Éster.
Os anidridos de ácidos carboxílicos são compostos que apresentam em sua estrutura química um átomo de oxigênio ligado a dois grupos carbonílicos com dois radicais orgânicos. Sobre os anidridos, marque a alternativa correta.
Se as duas moléculas de ácido carboxílico que formam o anidrido forem diferentes, o anidrido será chamado de simétrico.
Se as duas moléculas de ácido carboxílico que formam o anidrido forem iguais, o anidrido será chamado de assimétrico.
Os anidridos mistos são nomeados mantendo o nome de apenas um ácido carboxílico.
Os anidridos simétricos são nomeados pelo nome do ácido carboxílico correspondente.
A palavra anidrido significa com água.
As reações abaixo podem ocorrer através de substituições nucleofílicas do tipo Sn1 ou Sn2. A reação de substituição classificada como Sn1 ocorre via formação de carbocátion, e a Sn2, o nucleófilo faz o ataque por trás do grupo abandonador formando um produto com configuração invertida. Considerando os conceitos de substituição nucleofílica, com relação à classificação das reações 1 e 2 abaixo e a natureza do grupo abandonador cloro, pode-se afirmar que:

Sn2 e Sn1; o cloro sai na forma de Cl- pelo fato de ser uma base fraca.
Sn1 e Sn2; o cloro é um bom grupo abandonador, pois forma uma base estável.
Sn1 e Sn2; o cloro não é um bom grupo abandonador porque forma uma base instável.
Sn1 e Sn1; o cloro sai na forma de Cl- e pode ser considerado uma base forte.
Sn2 e Sn2; o cloro é um bom grupo abandonador, pois forma uma base estável.
Qual a ordem decrescente de reatividade em condições de SN2 para os seguintes substratos:
- 1-cloro-2-metilbutano
- 2-cloro-2-metilbutano
- 1-cloro-3metilbutano
- 1-cloro-pentano
1-cloro-2-metilbutano, 1-cloro-3-metilbutano, 2-cloro-2-metilbutano, 1-cloro-pentano
1-cloro-pentano, 1-cloro-2-metilbutano, 2-cloro-2-metilbutano, 1-cloro-3-metilbutano
1-cloro-3-metilbutano, 1-cloro-2-metilbutano, 2-cloro-2-metilbutano, 1-cloro-pentano
1-cloro-pentano, 1-cloro-3-metilbutano, 1-cloro-2-metilbutano, 2-cloro-2-metilbutano
2-cloro-2-metilbutano, 1-cloro-2-metilbutano, 1-cloro-3-metilbutano, 1-cloro-pentano
Os carbocátions são classificados de acordo com o número de substituintes que estão ligados ao carbono com a carga positiva. Sendo assim carbocátion primário possui apenas um substituinte alquila ligado ao carbono de carga positiva, carbocátion secundário possui dois substituintes ligados e carbocátion terciário possui três substituintes ao carbono com carga positiva. Sendo assim, podemos afirmar que a estabilidade do carbocátion:
Diminui com o aumento de substituintes ao carbono com carga positiva.
Aumenta com o aumento de substituintes ao carbono com carga positiva.
O carbocátion possui sempre a mesma estabilidade.
Aumenta com o menor número de substituintes ao carbono com carga positiva.
Aumenta com o aumento de substituintes ao carbono com carga negativa.
Para compreender as reações químicas orgânicas, devemos conhecer primeiramente alguns conceitos básicos, como diferenciar nucleófilos de eletrófilos. Sendo assim, analisando as espécies químicas a seguir:
 Podemos dizer que estas podem ser classificadas, respectivamente, como:
Podemos dizer que estas podem ser classificadas, respectivamente, como:
Radical livre, reagente nucleófilo, reagente nucleófilo, reagente eletrófilo.
Reagente nucleófilo, radical livre, reagente nucleófilo, reagente eletrófilo.
Reagente nucleófilo, reagente eletrófilo, reagente nucleófilo, radical livre.
Reagente eletrófilo, reagente nucleófilo, reagente nucleófilo, radical livre.
Reagente eletrófilo, radical livre, reagente nucleófilo, reagente nucleófilo.
Pelo conceito de Lewis, base é toda espécie química capaz de doar par de elétrons, enquanto que um ácido, é a espécie que está deficiente de elétrons e poderá receber esse par. Assinale, entre as alternativas abaixo, a fórmula de um composto que é uma base de Lewis:
Se as duas moléculas de ácido carboxílico que formam o anidrido forem diferentes, o anidrido será chamado de simétrico.
Se as duas moléculas de ácido carboxílico que formam o anidrido forem iguais, o anidrido será chamado de assimétrico.
Os anidridos mistos são nomeados mantendo o nome de apenas um ácido carboxílico.
Os anidridos simétricos são nomeados pelo nome do ácido carboxílico correspondente.
A palavra anidrido significa com água.
As reações abaixo podem ocorrer através de substituições nucleofílicas do tipo Sn1 ou Sn2. A reação de substituição classificada como Sn1 ocorre via formação de carbocátion, e a Sn2, o nucleófilo faz o ataque por trás do grupo abandonador formando um produto com configuração invertida. Considerando os conceitos de substituição nucleofílica, com relação à classificação das reações 1 e 2 abaixo e a natureza do grupo abandonador cloro, pode-se afirmar que:

Sn2 e Sn1; o cloro sai na forma de Cl- pelo fato de ser uma base fraca.
Sn1 e Sn2; o cloro é um bom grupo abandonador, pois forma uma base estável.
Sn1 e Sn2; o cloro não é um bom grupo abandonador porque forma uma base instável.
Sn1 e Sn1; o cloro sai na forma de Cl- e pode ser considerado uma base forte.
Sn2 e Sn2; o cloro é um bom grupo abandonador, pois forma uma base estável.
Qual a ordem decrescente de reatividade em condições de SN2 para os seguintes substratos:
- 1-cloro-2-metilbutano
- 2-cloro-2-metilbutano
- 1-cloro-3metilbutano
- 1-cloro-pentano
1-cloro-2-metilbutano, 1-cloro-3-metilbutano, 2-cloro-2-metilbutano, 1-cloro-pentano
1-cloro-pentano, 1-cloro-2-metilbutano, 2-cloro-2-metilbutano, 1-cloro-3-metilbutano
1-cloro-3-metilbutano, 1-cloro-2-metilbutano, 2-cloro-2-metilbutano, 1-cloro-pentano
1-cloro-pentano, 1-cloro-3-metilbutano, 1-cloro-2-metilbutano, 2-cloro-2-metilbutano
2-cloro-2-metilbutano, 1-cloro-2-metilbutano, 1-cloro-3-metilbutano, 1-cloro-pentano
Os carbocátions são classificados de acordo com o número de substituintes que estão ligados ao carbono com a carga positiva. Sendo assim carbocátion primário possui apenas um substituinte alquila ligado ao carbono de carga positiva, carbocátion secundário possui dois substituintes ligados e carbocátion terciário possui três substituintes ao carbono com carga positiva. Sendo assim, podemos afirmar que a estabilidade do carbocátion:
Diminui com o aumento de substituintes ao carbono com carga positiva.
Aumenta com o aumento de substituintes ao carbono com carga positiva.
O carbocátion possui sempre a mesma estabilidade.
Aumenta com o menor número de substituintes ao carbono com carga positiva.
Aumenta com o aumento de substituintes ao carbono com carga negativa.
Para compreender as reações químicas orgânicas, devemos conhecer primeiramente alguns conceitos básicos, como diferenciar nucleófilos de eletrófilos. Sendo assim, analisando as espécies químicas a seguir:
 Podemos dizer que estas podem ser classificadas, respectivamente, como:
Podemos dizer que estas podem ser classificadas, respectivamente, como:
Radical livre, reagente nucleófilo, reagente nucleófilo, reagente eletrófilo.
Reagente nucleófilo, radical livre, reagente nucleófilo, reagente eletrófilo.
Reagente nucleófilo, reagente eletrófilo, reagente nucleófilo, radical livre.
Reagente eletrófilo, reagente nucleófilo, reagente nucleófilo, radical livre.
Reagente eletrófilo, radical livre, reagente nucleófilo, reagente nucleófilo.
Pelo conceito de Lewis, base é toda espécie química capaz de doar par de elétrons, enquanto que um ácido, é a espécie que está deficiente de elétrons e poderá receber esse par. Assinale, entre as alternativas abaixo, a fórmula de um composto que é uma base de Lewis:

Sn2 e Sn1; o cloro sai na forma de Cl- pelo fato de ser uma base fraca.
Sn1 e Sn2; o cloro é um bom grupo abandonador, pois forma uma base estável.
Sn1 e Sn2; o cloro não é um bom grupo abandonador porque forma uma base instável.
Sn1 e Sn1; o cloro sai na forma de Cl- e pode ser considerado uma base forte.
Sn2 e Sn2; o cloro é um bom grupo abandonador, pois forma uma base estável.
Qual a ordem decrescente de reatividade em condições de SN2 para os seguintes substratos:
- 1-cloro-2-metilbutano
- 2-cloro-2-metilbutano
- 1-cloro-3metilbutano
- 1-cloro-pentano
1-cloro-2-metilbutano, 1-cloro-3-metilbutano, 2-cloro-2-metilbutano, 1-cloro-pentano
1-cloro-pentano, 1-cloro-2-metilbutano, 2-cloro-2-metilbutano, 1-cloro-3-metilbutano
1-cloro-3-metilbutano, 1-cloro-2-metilbutano, 2-cloro-2-metilbutano, 1-cloro-pentano
1-cloro-pentano, 1-cloro-3-metilbutano, 1-cloro-2-metilbutano, 2-cloro-2-metilbutano
2-cloro-2-metilbutano, 1-cloro-2-metilbutano, 1-cloro-3-metilbutano, 1-cloro-pentano
Os carbocátions são classificados de acordo com o número de substituintes que estão ligados ao carbono com a carga positiva. Sendo assim carbocátion primário possui apenas um substituinte alquila ligado ao carbono de carga positiva, carbocátion secundário possui dois substituintes ligados e carbocátion terciário possui três substituintes ao carbono com carga positiva. Sendo assim, podemos afirmar que a estabilidade do carbocátion:
Diminui com o aumento de substituintes ao carbono com carga positiva.
Aumenta com o aumento de substituintes ao carbono com carga positiva.
O carbocátion possui sempre a mesma estabilidade.
Aumenta com o menor número de substituintes ao carbono com carga positiva.
Aumenta com o aumento de substituintes ao carbono com carga negativa.
Para compreender as reações químicas orgânicas, devemos conhecer primeiramente alguns conceitos básicos, como diferenciar nucleófilos de eletrófilos. Sendo assim, analisando as espécies químicas a seguir:
 Podemos dizer que estas podem ser classificadas, respectivamente, como:
Podemos dizer que estas podem ser classificadas, respectivamente, como:
Radical livre, reagente nucleófilo, reagente nucleófilo, reagente eletrófilo.
Reagente nucleófilo, radical livre, reagente nucleófilo, reagente eletrófilo.
Reagente nucleófilo, reagente eletrófilo, reagente nucleófilo, radical livre.
Reagente eletrófilo, reagente nucleófilo, reagente nucleófilo, radical livre.
Reagente eletrófilo, radical livre, reagente nucleófilo, reagente nucleófilo.
Pelo conceito de Lewis, base é toda espécie química capaz de doar par de elétrons, enquanto que um ácido, é a espécie que está deficiente de elétrons e poderá receber esse par. Assinale, entre as alternativas abaixo, a fórmula de um composto que é uma base de Lewis:
1-cloro-2-metilbutano, 1-cloro-3-metilbutano, 2-cloro-2-metilbutano, 1-cloro-pentano
1-cloro-pentano, 1-cloro-2-metilbutano, 2-cloro-2-metilbutano, 1-cloro-3-metilbutano
1-cloro-3-metilbutano, 1-cloro-2-metilbutano, 2-cloro-2-metilbutano, 1-cloro-pentano
1-cloro-pentano, 1-cloro-3-metilbutano, 1-cloro-2-metilbutano, 2-cloro-2-metilbutano
2-cloro-2-metilbutano, 1-cloro-2-metilbutano, 1-cloro-3-metilbutano, 1-cloro-pentano
Os carbocátions são classificados de acordo com o número de substituintes que estão ligados ao carbono com a carga positiva. Sendo assim carbocátion primário possui apenas um substituinte alquila ligado ao carbono de carga positiva, carbocátion secundário possui dois substituintes ligados e carbocátion terciário possui três substituintes ao carbono com carga positiva. Sendo assim, podemos afirmar que a estabilidade do carbocátion:
Diminui com o aumento de substituintes ao carbono com carga positiva.
Aumenta com o aumento de substituintes ao carbono com carga positiva.
O carbocátion possui sempre a mesma estabilidade.
Aumenta com o menor número de substituintes ao carbono com carga positiva.
Aumenta com o aumento de substituintes ao carbono com carga negativa.
Para compreender as reações químicas orgânicas, devemos conhecer primeiramente alguns conceitos básicos, como diferenciar nucleófilos de eletrófilos. Sendo assim, analisando as espécies químicas a seguir:
 Podemos dizer que estas podem ser classificadas, respectivamente, como:
Podemos dizer que estas podem ser classificadas, respectivamente, como:
Radical livre, reagente nucleófilo, reagente nucleófilo, reagente eletrófilo.
Reagente nucleófilo, radical livre, reagente nucleófilo, reagente eletrófilo.
Reagente nucleófilo, reagente eletrófilo, reagente nucleófilo, radical livre.
Reagente eletrófilo, reagente nucleófilo, reagente nucleófilo, radical livre.
Reagente eletrófilo, radical livre, reagente nucleófilo, reagente nucleófilo.
Pelo conceito de Lewis, base é toda espécie química capaz de doar par de elétrons, enquanto que um ácido, é a espécie que está deficiente de elétrons e poderá receber esse par. Assinale, entre as alternativas abaixo, a fórmula de um composto que é uma base de Lewis:
Diminui com o aumento de substituintes ao carbono com carga positiva.
Aumenta com o aumento de substituintes ao carbono com carga positiva.
O carbocátion possui sempre a mesma estabilidade.
Aumenta com o menor número de substituintes ao carbono com carga positiva.
Aumenta com o aumento de substituintes ao carbono com carga negativa.
Para compreender as reações químicas orgânicas, devemos conhecer primeiramente alguns conceitos básicos, como diferenciar nucleófilos de eletrófilos. Sendo assim, analisando as espécies químicas a seguir:
 Podemos dizer que estas podem ser classificadas, respectivamente, como:
Podemos dizer que estas podem ser classificadas, respectivamente, como:
Radical livre, reagente nucleófilo, reagente nucleófilo, reagente eletrófilo.
Reagente nucleófilo, radical livre, reagente nucleófilo, reagente eletrófilo.
Reagente nucleófilo, reagente eletrófilo, reagente nucleófilo, radical livre.
Reagente eletrófilo, reagente nucleófilo, reagente nucleófilo, radical livre.
Reagente eletrófilo, radical livre, reagente nucleófilo, reagente nucleófilo.
Pelo conceito de Lewis, base é toda espécie química capaz de doar par de elétrons, enquanto que um ácido, é a espécie que está deficiente de elétrons e poderá receber esse par. Assinale, entre as alternativas abaixo, a fórmula de um composto que é uma base de Lewis:
Radical livre, reagente nucleófilo, reagente nucleófilo, reagente eletrófilo.
Reagente nucleófilo, radical livre, reagente nucleófilo, reagente eletrófilo.
Reagente nucleófilo, reagente eletrófilo, reagente nucleófilo, radical livre.
Reagente eletrófilo, reagente nucleófilo, reagente nucleófilo, radical livre.
Reagente eletrófilo, radical livre, reagente nucleófilo, reagente nucleófilo.